Revisión del Anexo 1: Momento para entender la diferencia entre esterilización y biodescontaminación.
Introducción: la problemática del draft del Anexo 1 en torno al VH2O2 para ‘esterilizar superficies’
Como muchos de vosotros ya sabréis, el draft del nuevo Anexo 1 (v12) cuestiona los ciclos de peróxido de hidrógeno vaporizado (VHP/VH2O2) como método de esterilización superficial para partes de contacto indirecto con el producto. Se argumenta que el VH2O2 no tiene capacidad de penetración y que la esterilización implica poder penetrar para asegurar el nivel de esterilidad. Lo cierto es que los ciclos VHP/VH2O2 muestran cierta fragilidad y a veces se detectan indicadores positivos de forma inesperada. En la farmacopea EU no existe referencia explícita al VH2O2 como método de esterilización de superficies. En cambio, sí que existen referencias en las USP o incluso artículos de la PDA que avalan el uso del peróxido para esterilizar o descontaminar superficies.
Section 5.5 “Direct and indirect contact parts should be sterilized. Direct contact parts are those that the product passes through, such as filling needles or pumps. Indirect product contact parts are equipment parts that come into contact with sterilized critical items and components”
Section 8.12 “For sterile products that cannot be filtered, the following should be considered: i. All product and component contact equipment should be sterilized prior to use.”
In the case where vH202/VHP cycle is applied as the only bio-decontamination process for the barrier and process equipment non-product contact surfaces and in the same cycle ‘surface sterilization’ of in-direct product contact parts this would have to be justified using QRM principles. Such principles would need to recognize the different requirements for cleaning and bioburden control for bio-decontamination of non-product-contact process equipment/ barrier surfaces and ‘surface sterilization’ of in-direct product contact surfaces.

En el contexto del llenado aséptico, si descartamos el VH2O2 como esterilización superficial, esto conlleva necesariamente a una esterilización “out of place” en autoclave: desmontar tolvas de alimentación, guías y demás de dentro del aislador, llevarlas a una autoclave para esterilizar y después, montarlas de nuevo tratando de no contaminarlas.
Esta situación puede implicar problemas como que la cámara de la autoclave no tenga suficiente capacidad o esté dimensionada para la tolva, que haya que desarrollar nuevos PNTs, formar y cualificar operarios, pérdida de productividad por paro de línea, etc. Un auténtico quebradero de cabeza.
Foto: Cortesía de Dara Pharmaceutical Packaging
Diferencias entre esterilización y biodescontaminación
Este artículo trata de esclarecer los conceptos de esterilización y biodescontaminación para entender problema y tratar de buscar soluciones.
1. Conceptos de estéril, esterilidad y esterilización
El primer término es un concepto binario. Una cosa, o es estéril o no lo es. No puede ser “medio estéril”. Por estéril entendemos aquel producto con ausencia total de partículas viables.
En cuanto al segundo término, esterilidad o nivel del aseguramiento de la esterilidad (SAL), es un concepto microbiológico que designa la probabilidad de que un producto sometido a un proceso de esterilización contenga un microorganismo viable. Esta probabilidad es, por definición, 10e-6.
¿Y qué significa esterilización? Según la norma ISO 14161 de Esterilización de productos sanitarios, esterilización es aquel proceso que puede validarse partiendo de una carga microbiana de 10e6 hasta alcanzar el SAL de 10e-6. Esto significa literalmente que un proceso de esterilización debe conseguir en realidad una reducción de 12-log.
En la práctica, es imposible comprobar tal eficacia. ¿Por qué? Porque para demostrarlo empíricamente se deberían fabricar 1 millón de muestras, inocular cada una de ellas con poblaciones de esporas 10e6 y realizar pruebas de esterilidad de todas y cada una de ellas. Como esto es prácticamente imposible, los microbiólogos utilizan datos empíricos y fórmulas matemáticas para calcular el efecto letal del calor y del tiempo necesario en un proceso de esterilización para asegurar el SAL.
2. Biodescontaminación
Algunos estudios han determinado que el VH2O2 tiene una capacidad de penetración de tan solo 10-20 nm. Una espora de Bacillus stearothermopillus mide hasta 3 µm de largo y 1 µm de ancho. A veces, durante la fabricación de los indicadores, se producen aglomeraciones (“clumping”) de esporas y entonces el peróxido no podrá penetrar más allá de la primera capa. Esto da lugar a que el indicador resulte positivo, independientemente de que el proceso consiga una buena distribución y contacto con todas las superficies. A estos indicadores se los denomina “rogue BI” porque dan un resultado falso. Falso en cuanto a que el peróxido ha contactado con la superficie, pero cierto en cuanto a que el positivo se debe a que no ha sido capaz de penetrar hacia adentro. De ahí la fragilidad de los ciclos VH2O2 y el motivo por el que no puede considerarse un proceso de esterilización. En el caso esterilización en autoclave, esto no pasaría ya que, en condiciones de presión y temperatura a 121°C, el vapor penetra perfectamente hasta el fondo y estos indicadores resultarían negativos. Por este motivo, en los procesos o ciclos VH2O2 deberíamos emplear la palabra ‘biodescontaminación’ y no ‘esterilización’, que se reserva a procesos penetrantes.
3. Limpieza, bioburden y análisis de riesgos
¿Quiere esto decir que en las superficies es imposible conseguir un nivel SAL (10-6) con VH2O2? Pues en teoría, no. Para conseguirlo, el proceso de limpieza y sanitización de superficies debería reducir la contaminación (bioburden) a una monocapa de microorganismos. El nuevo anexo nos dice que, si el ciclo VHP/VH2O2 se utiliza para descontaminación del aislador y máquina de llenado en aquellas partes sin contacto directo con producto y queremos aprovecharlo como esterilización superficial de partes en contacto indirecto, deberíamos utilizar técnicas QRM o de análisis de riesgos (ver la cita de arriba en negrita) para esas partes más críticas, poniendo empeño en el estudio de limpieza y bioburden.
Buscando soluciones
En cierta manera, si conseguimos sanitizar a niveles de bioburden <10e3 y diseñar un proceso de biodescontaminación VH2O2 de 9-log, el proceso conseguiría niveles de esterilidad (10-6). Desgraciadamente, no existen indicadores con poblaciones de 10e9 para validar estos procesos. Pero recientemente, en el Congreso de Microbiología Rápida organizado por A3P Comité España se debatió acerca del uso de técnicas innovadoras de microbiología para asegurar mejor los procesos asépticos. Uno de los ponentes, el consultor Gilberto Dalmaso, defendió que los microbiólogos farmacéuticos deberían tomar la iniciativa e innovar en este aspecto. También expuso que el mismo Draft V12 del Anexo 1 anima a utilizar métodos de microbiología rápida con esta frase: “El uso de tecnologías apropiadas (P.ej. RABS, Aisladores, sistemas Robotizados y sistemas de monitorización ambiental y/o pruebas de microbiología rápida) deberían ser consideradas para aumentar la protección del producto versus contaminación de personal, materiales, …”. Veremos como queda finalmente pero ya es hora de sacar provecho de las tecnologías innovadoras de microbiología rápida. Una de ellas son los indicadores enzimáticos. Estos indicadores permiten cuantificar el efecto letal del peróxido correlacionando la mortalidad de una población de esporas con la actividad remanente (RLU) del enzima Adenilato Kinasa (tAK). Ciertamente, implementar un proceso así requiere realizar múltiples pruebas y generar datos durante un tiempo para poderlo validar. No obstante, el beneficio en forma de productividad y disminución de riesgos compensa sobradamente el esfuerzo y algunas empresas multinacionales ya están aprovechando las ventajas de esta herramienta.
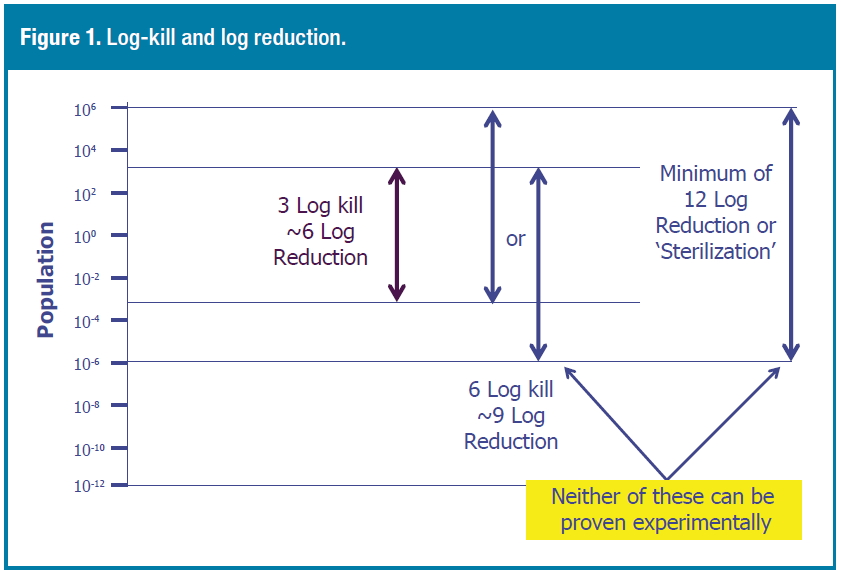
Este gráfico, tomado del artículo «Real-World Vapor Phase Hydrogen Peroxide Decontamination» de James Agalloco, es muy ilustrativo para aclarar conceptos. Como se ha comentado, ni la reducción de 9-log ni la reducción de 12-log para lograr un SAL 10e-6 se pueden probar experimentalmente. En el caso de esterilización, confiamos en la capacidad de penetración del vapor para garantizar que se haya alcanzado SAL 10e-6, mientras que, con la biodescontaminación, suponiendo una carga biológica máxima de 10e3 deberíamos desarrollar un ciclo que alcanzara una reducción de 9-log para tener un nivel de letalidad de 6-log (o SAL 10e-6).
Conclusión
Biodescontaminación y esterilización son procesos análogos que implican aniquilar poblaciones de microorganismos, pero tienen connotaciones distintas. La esterilización es penetrante y ello ofrece la confianza necesaria para la consecución del nivel de esterilidad (10e-6) según los cálculos de los microbiólogos. En cambio, la biodescontaminación es un proceso más frágil porque es superficial. No ofrece tal confianza y requiere mayor atención. Por ello, es necesario realizar estudios de bioburden en las zonas más críticas y desarrollar ciclos robustos. Para validar un nivel de biodescontaminación cercano a la esterilidad, deberemos demostrar que nuestro proceso de limpieza y sanitización consigue un bioburden bajo (<10e3) y realizar luego un ciclo VH2O2 que permita reducir hasta 9-log. Los indicadores enzimáticos, que forman parte del grupo de técnicas de microbiología rápida/alternativa, son la herramienta perfecta para apoyar estudios de reducción logarítmica superiores a 6-log y ayudar a validar tales procesos.